연구소소개
-
36
KIST, 공간과 장소를 기억하는 원리 밝혔다
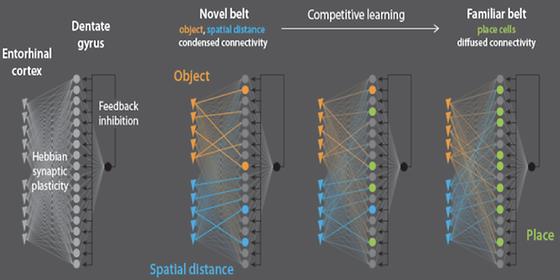
- 해마 속 과립세포의 위치정보를 기억하는 장소세포가 공간을 기억하도록 변화 - 해마의 역할을 이해함으로써, 기억 관련 네트워크 모델링 해마 손상 관련 뇌질환 이해 새로운 도시를 방문하면 모든 게 낯설게 느껴지고 건물들과 주변 지표들을 확인해가며 길을 잃지 않도록 신경을 쓰게 된다. 하지만 점차 익숙해지면 주변 지표들을 굳이 일일이 확인하지 않아도 길을 헤매는 일은 없어진다. 이런 학습을 통한 공간 기억이 생기는 원리를 국내 연구진이 밝혔다. 뇌의 영역 중 해마는 주변 환경과 자신의 위치 정보를 제공하며 새로운 사실을 학습하고 기억하는 기능을 하는 중요한 기관이다. 알츠하이머와 같은 뇌질환이 진행될 때 가장 먼저 손상되는 곳이기도 하다. 세포의 활동을 통해 위치를 인지할 수 있는 장소 세포 발견 이후 뇌의 위치추적 메커니즘이 점차 규명되었으며 공간의 탐색과 기억에 대한 많은 연구들이 발표되었다. 하지만 공간에 익숙해지면서 기억하게 되는 장소 세포가 어떻게 생성 되며 변화 하는지는 밝혀지지 않았었다. 한국과학기술연구원(KIST, 원장 윤석진)은 뇌과학운영단 세바스쳔 로열 박사팀이 해마 속 과립세포가 이끼세포 등 다양한 신경 네트워크를 통해 장소를 학습하게 되는 원리를 규명했다고 밝혔다. KIST 세바스쳔 로열 박사팀은 해마의 장소 정보 입력이 시작되는 부위로 알려진 치아이랑의 뇌 세포를 관찰하여 새로운 환경을 학습하면서 장소 세포가 생성되는 과정을 연구 하였다. 공간훈련장치인 트레드밀에서 실험용 생쥐를 27일 동안 훈련하며 치아이랑을 구성하는 뇌세포인 이끼세포와 과립세포의 변화를 관찰하였다. 장소를 기억하는 여러 특성을 갖고 있는 과립세포를 관찰한 결과, 새로운 공간에 놓였을 때 과립세포 내에 존재하는 장소세포는 사물의 위치 정보를 나타내거나 일정한 간격의 거리의 정보를 나타냈다. 점차 공간에 익숙해지고 학습된 후에는 사물의 위치 정보와 거리 정보를 나타내는 세포들은 소멸되고 특정 장소를 나타내는 장소세포들이 점차 늘어났다. KIST 연구진은 이러한 학습에 따른 점진적 세포 활동의 변화를 신경망 모델중 하나인 경쟁학습 모델을 통해 재현하였고, 이끼세포 또한 과립세포와 상호작용을 통해 장소 기억에 관여함을 밝혔다. 이끼세포 자신은 공간 학습에 따른 큰 변화는 없었지만 이끼세포의 활동이 과립세포가 사물 위치 정보에서 공간의 위치기억으로 변화하는데 큰 역할을 한다고 밝혔다. KIST 세바스쳔 로열 박사는 “해마의 역할을 이해하는데 크게 공헌함으로써 인공지능 기반의 신경공학에 기여할 뿐 아니라 기억 상실, 알츠하이머, 인지장애와 같은 해마의 손상과 관련된 뇌질환을 이해하고 치료 예방하는데 새로운 방향을 제시할 수 있을 것이다.”라고 밝혔다. 본 연구는 과학기술정보통신부(장관 최기영) 지원으로 KIST 주요사업으로 수행되었으며, 연구결과는 ‘Nature Communications’ (IF: 12.12, JCR 분야 상위 7.75%) 최신호에 게재되었다. * (논문명) Place cell maps slowly develop via competitive learning and conjunctive coding in the dentate gyrus - (제 1저자) 한국과학기술연구원 김소연 박사후연구원 - (교신저자) 한국과학기술연구원 세바스쳔 로열 <그림설명> [그림1] 트레드밀 학습 중 세포 활동 기록 [그림2] 트레드밀 학습을 위한 컴퓨터 모델
- 35
- 작성자기능커넥토믹스연구단 정다희 박사팀
- 작성일2020.09.30
- 조회수8599
-
34
KIST, 망막 변성 환자들에 필요한 인공 시각 성능향상의 실마리 발견했다
- 유전자 조작 쥐 실험 통해 망막 변성 진행에 따른 신경 신호 변화 확인 - 인공 망막 장치 이식 대상자 선정에 대한 가이드라인 제시 기대 국내 연구진이 인공 망막 장치의 성능을 향상시킬 실마리를 찾았다. 한국과학기술연구원(KIST, 원장 직무대행 윤석진) 바이오마이크로시스템연구단 임매순 박사팀은 하버드 의대 Shelley Fried 교수팀과의 공동 연구를 통해 망막 질환의 진행 정도에 따른 인공 시각 신경 신호 변화 패턴을 확인했다고 밝혔다. 망막 색소 변성 및 노인성 황반 변성 등의 망막 변성 질환은 빛을 전기화학적 신경 신호로 변환해주는 광수용체 세포들을 파괴하여 시력을 잃게 되는 질병이다. 해당 질병들은 치료 약물이 존재하지 않고, 구조가 상대적으로 간단한 각막이나 수정체와 달리 복잡한 신경 조직인 망막은 이식이나 교체가 불가능하다. 다행히 광수용체 세포 뒷단에서 뇌로 신경 신호를 전달하는 신경절 세포들은 살아남기 때문에, 안구 내에 마이크로 전극을 이식하여 전기적으로 자극하면 인공 시각을 형성할 수 있다. 이러한 원리로 동작하는 인공 망막 장치는 망막 변성 질환으로 실명한 환자들의 유일한 시력 회복 방법이다. 하지만, 이식받은 환자마다 큰 성능 차이를 보이는데 그 원인을 알지 못해 일반적으로 적용하기 어려운 상황이다. KIST 연구진은 사람의 망막 색소 변성과 비슷한 양상으로 실명하게 된 유전자 조작 실험용 쥐에서 인공 망막 사용자 간의 성능 차이를 설명할 수 있는 실험결과를 얻었다. 지금까지는 정상 망막이나 심하게 질병이 진행된 망막에서 연구가 이루어져 왔으나, 연구진은 질병이 진행되는 과정에서 인공 시각 신경 신호 변화를 확인할 수 있도록 체계적인 실험을 수행했다. 그 결과, 망막 변성이 진행됨에 따라 전기 자극에 대한 신경 신호의 크기와 일관성이 감소하는 것을 확인하였다. 인공 망막 장치는 반복적인 전기 자극으로 인공 시각 이미지를 주기적으로 갱신한다. 이 때문에 일관된 신경 신호를 받는 것이 중요하다. 예를 들어, 사용자가 알파벳 ‘K’를 계속 응시하는 동안에는 반복되는 전기 자극들이 모두 ‘K’를 의미하는 신경 신호를 형성해야 해당 글자를 인지할 수 있다. 그러나, 변성 망막에서 일관성이 낮아지게 되면, ‘K’를 바라보고 있는데도 각각의 전기 자극이 ‘L’, ‘R’, ‘S’ 등 서로 다른 알파벳을 나타내는 신경 신호를 뇌로 전달하여 무엇을 보고 있는지 해석하기 어렵게 되는 것이다. KIST 연구진의 실험에서는 각 신경 세포에 동일한 전기 자극을 여러 번 반복했을 때 발생하는 신경 신호가 서로 얼마나 비슷한지 평가하였는데, 정상 망막에서는 신경 신호가 매우 비슷하여 높은 일관성을 보였으나 망막 변성이 진행됨에 따라 일관성이 크게 감소하는 것이 확인되었다. 제 1저자인 윤영준 박사와 이재익 박사는 “변성된 망막에서는 시선을 고정하고 있더라도 계속 서로 다른 신경 신호가 뇌로 전달되어 전기 자극으로 만들어진 인공 시각 정보 인지를 저하시키는 원인이 되는 것으로 보인다.”라고 밝혔다. KIST 임매순 박사는 “망막 변성 질환들은 환자에 따라 그 질병의 경과가 다른 것으로 알려져 있고, 인공 망막 장치를 이식받을 대상의 망막 상태도 매우 다를 수 있다. 따라서, 좋은 품질의 인공 시각을 위해서는 망막 변성 진행 정도를 면밀히 검토하여 인공 망막 장치 이식 대상 및 시기를 결정해야 한다는 것을 의미한다.”라며, “변성이 많이 진행된 망막에서도 우수한 인공 시각을 형성하기 위해 신경 신호 일관성을 높이기 위한 연구를 다방면으로 진행하고 있다.”라고 말했다. 본 연구는 과학기술정보통신부(장관 최기영) 지원으로 KIST 주요사업과 한국연구재단 신진연구자지원사업으로 수행되었으며, 연구 결과는 ‘IEEE Transactions on Neural Systems and Rehabilitation Engineering’ 최신호에 게재되었다. * (논문명) Retinal Degeneration Reduces Consistency of Network-mediated Responses Arising in Ganglion Cells to Electric Stimulation - (제 1저자) 한국과학기술연구원 윤영준 위촉연구원 - (제 1저자) 하버드 의대 매사추세츠 종합병원 이재익 박사후연구원 - (교신저자) 한국과학기술연구원 임매순 선임연구원 <그림설명> [그림 1] (위) 인공 망막 장치 이식 및 인공 시각 신경 신호에 의한 뇌 시각 피질의 활성화 개념도 (중간) 정상 망막은 반복적인 전기 자극에 대해 비슷한 신경 신호를 뇌로 전달하여 시각 정보(예시-KIST 글씨)를 사용자가 정확하게 인지할 수 있음. (아래) 변성 망막에서는 동일 전기 자극에도 서로 다른 신경 신호가 뇌로 전달되어 시각 정보를 정확하게 인지하지 못함. [그림 2] 망막 변성 질환 진행 정도에 따른 신경 신호 일관성 실험 결과. 동일 전기 자극을 7번 반복적으로 인가하고 각각이 형성한 신경 신호가 서로 비슷한 정도(Inter-trial correlation)를 STTC(Spike Time Tiling Coefficient) 값을 계산하여 비교 분석함. 위 그래프에서는 붉은색이 많을수록 일관성이 높고, 알록달록해질수록 일관성이 낮아짐을 나타냄. 아래 그래프에서는 STTC 값이 작아질수록 일관성이 낮아짐을 의미. 두 그래프 모두에서 정상 쥐의 망막(wt, wild-type)과 망막 변성 쥐의 질병 시작 전(P15, 생후 15일)에는 높은 신경 신호 일관성을 보이나, 망막 변성 쥐가 나이 들어감에 따라 (질병이 진행됨에 따라) 일관성이 크게 낮아지는 것이 확인됨.
- 33
- 작성자바이오마이크로시스템연구단 임매순 박사팀
- 작성일2020.07.17
- 조회수8091
-
32
KIST 뇌과학 연구팀, 고혈압 원인인자 밝혔다. 심장의 혈압 감지 유전자 발견
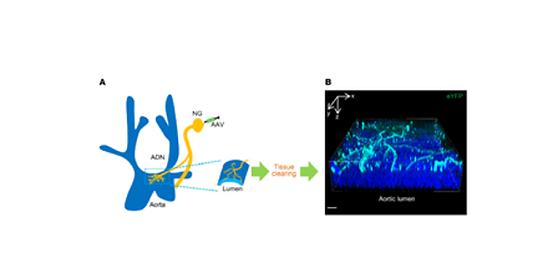
- 막단백질(기계채널) 텐토닌3의 심장에서 혈압 감지 역할 밝혀 - 고혈압 등 혈압 관련 질병의 이해 및 치료제로의 발전 가능성 기대 고혈압은 뇌졸중, 심장마비 등을 일으키는 현대인의 고질적인 질병 중 하나이다. 우리가 직접 감지하지는 못해도 우리의 몸은 동맥의 혈압을 측정하고, 혈압이 너무 낮으면 높이고 반대로 혈압이 높으면 낮추며 조절하고 있다. 혈압 조절이 잘되지 않으면 대개 고혈압으로 이어진다. 이렇게 혈압을 감지하는 센서 역할을 하는 세포를 혈압수용체라 부르는데, 그동안 혈압수용체 세포 내부의 어떤 단백질이 외부의 자극을 감지하는지는 알려지지 않았다. 한국과학기술연구원(KIST, 원장 직무대행 윤석진)은 뇌과학연구소 오우택 박사 연구팀이 근육의 수축과 이완을 조절하는 기계채널 단백질인 ‘텐토닌3’가 심장의 혈압 또한 정밀하게 조절하는 센서로 작용한다는 것을 밝혔다고 발표했다. 이온채널은 생체막에 통로를 형성하여 생체막 내외의 이온을 통과시키는 단백질로써, 이온의 이동에 따라 생체에 전기신호를 발생시킨다. 이온채널에 의한 세포의 전기적 흥분은 심장 박동, 호르몬 분비, 감각 및 운동을 가능하게 한다. 따라서, 이온채널이 고장나면 심각한 질병이 발생할 수 있다. 특히 이온채널 중 하나인 기계채널은 세포에 물리적(기계적) 자극이 가해질 때 열리는 이온채널로, 기계적 자극을 감지하는 생체센서이다. 따라서 기계채널은 촉각, 진동, 압각 등의 외부적인 자극을 감지하는데 사용될 뿐 아니라 근육의 수축정도, 뼈의 움직임, 허파 팽창, 혈압의 높낮음과 같은 내부의 자극을 감지하는데에도 필요하다. KIST 연구진은 혈압을 조절하는 센서를 파악하기 위해 심장 근방의 신경다발을 관찰하던 중 대동맥 혈압수용체 신경 말단에서 기계채널 텐토닌3의 유전자를 다량 발견하였다. 특히, 텐토닌3을 발현하는 신경은 대동맥을 완전히 싸고 있었다, 이에 KIST 오우택 박사는 텐토닌3 유전자를 제거한 쥐를 통해 실험한 결과, 혈압 감지 능력이 크게 떨어지는 것을 확인하였다. 또한, 텐토닌3 유전자를 다시 발현시켰더니 혈압이 원상태로 돌아오는 것을 확인하였다. KIST 뇌과학연구소 오우택 박사는 “심장의 혈류를 감지하여 혈압을 조절하는 텐토닌3 이온채널의 역할을 조명하였고, 동물의 혈압 감지 시스템의 생리학적인 이해의 범위를 한층 넓혔다 할 수 있다.”라며, “텐토닌3 이온채널 유전자의 역할을 명확하게 밝힌 본 연구를 통하여 심장 혈압감지의 오류로 인한 고혈압 치료에 초석이 되는 데 큰 역할을 할 것으로 생각한다.”라고 밝혔다. 본 연구는 과학기술정보통신부(장관 최기영) 지원으로 한국연구재단 뇌과학원천기술개발사업, 리더연구자지원사업을 통해 수행되었으며, 연구결과는 JCI(The Journal of Clinical Investigation, U.S.A.) (IF : 12.28, JCR 상위 : 1.84%) 최신호에 게재되었다. * (논문명) Tentonin 3/TMEM150C senses blood pressure changes in the aortic arch - (제 1저자) KIST 뇌과학연구소장실 Lu Huan-Jun 학생연구원 - (교신저자) KIST 뇌과학연구소 오우택 책임연구원 <그림설명> [그림 1] 대동맥 신경말단에서 텐토닌3의 발현 확인 [그림 2] 텐토닌3을 제거한 마우스는 혈압이 증가(A, B)하고 심박수(C)가 증가함 [그림 3] 심장에서 나오는 혈류의 혈압을 감지하는 기계채널과 관련 분자센서 모식도 (TTN3: 텐토닌3)
- 31
- 작성자뇌과학연구소 오우택 박사팀
- 작성일2020.07.10
- 조회수8154
-
30
KIST, 신규 치매 플랫폼 개발 머릿 속 치매 원인물질을 초기 단계부터 관찰한다
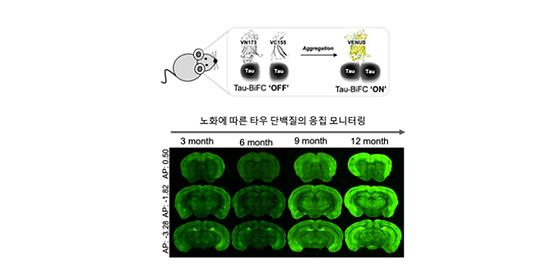
- 비정상적 타우 단백질 응집을 초기 단계부터 관찰할 수 있는 동물 모델 개발 - 타우 표적 치매 치료제 개발 연구 가속화 및 새로운 치매 기전 규명 기대 한국과학기술연구원(KIST, 원장 직무대행 윤석진) 치매DTC융합연구단 김윤경, 임성수 박사 연구팀은 치매 유발 원인으로 알려진 타우 단백질의 응집을 초기 단계부터 관찰할 수 있는 동물모델을 개발했다고 밝혔다. 이 신규 플랫폼을 활용하면 치료제 개발연구를 가속화하고, 새로운 치매 기전을 규명할 수 있을 것으로 기대된다. 가장 흔한 퇴행성 뇌질환인 알츠하이머성 치매는 뇌 속 베타-아밀로이드 단백질이나 타우 단백질이 응집되는 것이 주요 원인으로 여겨지고 있다. 잘 알려진 베타-아밀로이드의 응집은 뇌 기능이 손상되는데 길게는 십 년 이상이 걸리기도 하며 심지어 병변이 나타나지 않는 때도 있어, 최근 신경세포사멸에 직접적인 영향을 미치는 타우 단백질이 치매의 새로운 치료 표적으로 급부상하고 있다. 타우 단백질이 응집되기 시작하면, 단백질이 뭉친 형태인 올리고머 형태가 되는데, 이는 신경세포 독성을 일으키고 알츠하이머성 치매를 비롯한 다양한 퇴행성 뇌 질환을 전이시키는 매개체로써 작용한다. 이에 타우 올리고머를 표적으로 한 치매 치료제 개발이 화두에 오르고 있지만, 신경세포 내 과량으로 존재하는 정상 타우 단백질로부터 응집 초기에 소량으로 존재하는 타우 올리고머를 구분해낼 실험 방법이 부재한 상황이다. KIST 김윤경, 임성수 박사 연구팀은 세포에서 타우 올리고머의 형성을 관찰할 수 있는 플랫폼인 ‘타우-BiFC(Bimolecular Fluorescence Complementation) 플랫폼’을 확립하여 이를 동물모델로 확장한 ‘타우-BiFC 생쥐모델’을 개발하였다. 이 플랫폼은 신경세포 내에서 타우 단백질이 응집하여 올리고머가 형성되면 형광이 켜지는 시스템으로, 타우 응집 초기 올리고머 단계부터 정량적으로 관찰할 수 있다는 장점이 있다. KIST 연구진은 개발한 ‘타우-BiFC 생쥐’를 통해 단계별로 정량적인 모니터링이 가능했다. 생쥐가 어린 나이일 때 타우 올리고머가 생성되어도 세포 자체적으로 분해·제거하는 시스템이 가동되지만, 생쥐가 나이가 들수록 그 기능이 떨어져 타우의 응집이 가속되고 신경이 퇴화하는 특성을 보이는 것을 관찰할 수 있었다. KIST 김윤경 박사는 “타우-BiFC 생쥐모델은 뇌에 쌓이는 타우 단백질의 초기 응집 단계인 올리고머부터 효과적으로 관찰할 수 있는 신규 플랫폼으로, 외국에서 개발된 생쥐모델에 의존하던 기존의 치매 연구를 탈피할 수 있을 것”이라고 말하며, “신경세포 독성 및 전이성을 보이는 타우 응집체의 형성을 파악하고 관찰하는 연구는 알츠하이머성 치매를 포함한 타우 병증의 치료제 개발에 있어 중요한 시작점이라 할 수 있다.”라고 말했다. 본 연구는 과학기술정보통신부(장관 최기영) 지원으로 미래선도형융합연구단사업과 뇌과학원천기술개발사업 등으로 수행되었으며, 이번 연구결과는 신경과학 분야 국제 저널인 ‘Progress in Neurobiology’ (IF: 10.65, JCR 분야 상위 4.68%) 최신 호에 게재되었다. * (논문명) Visualization of soluble tau oligomers in TauP301L-BiFC transgenic mice demonstrates the progression of tauopathy - (제 1저자) 한국과학기술연구원 신슬기 박사과정 (UST) - (교신저자) 한국과학기술연구원 임성수 선임연구원 - (교신저자) 한국과학기술연구원 김윤경 책임연구원 <그림설명> [그림 1] 타우-BiFC 생쥐모델의 뇌에서 노화에 따른 타우 응집 정도 모니터링
- 29
- 작성자치매DTC융합연구단 김윤경 박사팀
- 작성일2020.04.21
- 조회수7575
-
28
KIST-가톨릭대 공동연구진, 다양한 바이러스에 적용 가능한 백신 플랫폼 개발
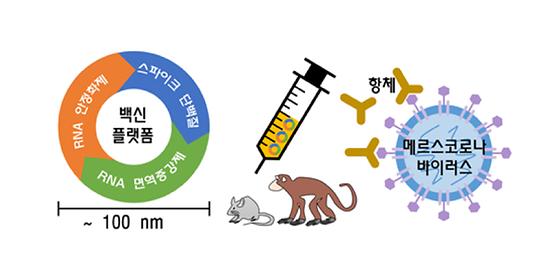
- RNA 면역증강제를 활용한 메르스 바이러스 백신 개발, 영장류 효과 확인 - 동일 계열인‘코로나 19’바이러스에 대한 안전한 백신 조기개발 기대 2015년 우리나라 전역을 공포로 뒤덮은 메르스는 2019년 발생한 코로나 19 (질환: COVID-19, 바이러스: SARS-CoV2)와 같은 계열의 코로나 바이러스(메르스 코로나 바이러스, MERS-CoV)에 의해 발병했다. 최근 국내 연구진이 메르스 코로나 바이러스에 대해 RNA 기반의 면역증강제를 활용한 새로운 백신 플랫폼을 개발했다고 밝혔다. 이번 연구는 영장류 실험을 마쳤으며, 현재 전 세계에 걸쳐 시급한 백신 개발이 요구되는 코로나 19에 적용이 가능할 것으로 기대된다. 한국과학기술연구원(KIST, 원장 직무대행 윤석진) 뇌의약연구단 금교창 단장, 방은경 박사 연구팀은 가톨릭대학교(가톨릭대, 총장 원종철) 남재환 교수 연구팀과의 공동연구를 통해 메르스 코로나바이러스(MERS-CoV)에 대한 RNA 기반의 백신 플랫폼에 대한 연구결과를 발표했다. 이 백신 플랫폼은 RNA를 면역증강제로 활용하고, 이 RNA를 안정적으로 유지시키는 화합물 및 코로나 바이러스가 숙주에 침투하는 스파이크 단백질(spike, 침투돌기 단백질)로 구성되어 있다. 이번 새로운 백신 플랫폼을 통해 동일한 바이러스 계열인 코로나 19 치료용 백신 개발에 활용될 것으로 기대된다. 최근, 우수한 안전성을 지녔다고 평가받는 단백질 기반 백신이 주로 개발되고 있다. 그러나 이러한 단백질 기반의 백신은 항체 생산의 세포에 대한 면역유도가 약하여 균형 잡힌 면역반응을 위해 반드시 안정성 높은 면역증강제를 사용해야 한다. 공동연구진은 가톨릭대학교 연구팀에서 면역증강제로 개발한 귀뚜라미 마비증세를 유발하는 바이러스의 RNA와 KIST 연구진이 개발한 아연 금속을 활용한 RNA 안정제를 혼합한 후, 코로나 바이러스 스파이크 단백질과 함께 면역하였다. 그 결과 실험 쥐를 대상으로 1회 접종만으로도 충분한 방어 면역 효능(치사량 바이러스 공격에 100% 방어효능을 보임)을 보였으며, 영장류인 마카큐 원숭이에서도 높은 중화항체(80% 억제 기준으로 1:2,560 희석배수)를 유도하여 코로나바이러스의 감염을 억제할 수 있음을 확인하였다. 이렇게 RNA 면역증강제와 안정제를 함께 면역하면 기존에 활용되고 있는 단백질 기반 백신이나 불활화 백신 등 대부분의 백신 타입에 적용할 수 있기 때문에 넓은 활용 가능성을 보여주고 있다. 공동연구진은 국제백신연구소 송만기 박사팀에서 코로나바이러스 스파이크 단백질을 제공받았고, 전북대학교 이상명 교수팀에서 바이러스 감염을 막을 수 있는 항체량( 중화항체가 : 항원 혈청의 단위용량에 포함되어있는 바이러스 감염을 억제할 수 있는 항체량의 측정값 중화항체가) 측정 및 바이러스 공격 실험을 진행했으며, 한국생명공학연구원 국가영장류센터 홍정주 박사팀에서 영장류(원숭이) 면역을 조사하였다. KIST 금교창 단장은 “메르스 바이러스에서 효과를 보인 이번 RNA를 활용한 단백질 기반 백신은 동일 계열인 코로나 19의 백신 개발에 신속히 적용할 수 있다는 장점이 있다.”라고 밝혔으며, 가톨릭대 남재환 교수는 “최근에 보고되는 핵산(DNA 혹은 RNA) 기반 백신은 실제 백신 제품으로 생산되어 대규모로 임상에 적용되어 본적이 없다. 그러나 본 연구에서 개발된 백신은 이미 안전성이 검증된 단백질 백신을 기반으로 하여 RNA를 면역증강제로 첨가한 새로운 백신 플랫폼이기 때문에 좀 더 안전한 백신 개발이 가능할 것으로 전망한다.”라고 밝혔다. 현재, 가톨릭대학교 연구팀은 동일한 백신 플랫폼을 활용하여 코로나 19 치료용 백신과 중증열성혈소판감소증후군 예방용 백신을 개발 중(연구비 지원 : ㈜삼광랩트리)이며, 공동 연구팀과 함께 SK 바이오사이언스와 컨소시엄을 구성하여 코로나 19 예방용 백신 개발을 진행 중이다. 이 연구는 보건복지부(장관 박능후) 지원으로 감염병위기대응백신기술개발 사업, 과기정통부(장관 최기영) 지원의 KIST 주요사업, 차세대신약기반기술개발사업 등으로 수행되었다. 이 연구 결과는 화학분야 저명 저널인 ‘Angewandte Chemie’ (IF : 12.257, JCR 분야 상위 9.593%) 최신호에 게재되었다. * (논문명) Nanoformulated Single-stranded RNA-based Adjuvant with a Coordinative Amphiphile as an Effective Stabilizer to Induce a Humoral Immune Response by Activation of Antigen presenting Cells - (제 1저자) 한국과학기술연구원 방은경 선임연구원 - (제 1저자) 가톨릭대학교 박효정 연구교수, 고해리 연구원 - (제 1저자) 한국생명공학연구원 홍정주 선임연구원 - (제 1저자) 전북대학교 이상명 교수 - (교신저자) 한국과학기술연구원 금교창 책임연구원 - (교신저자) 가톨릭대학교 남재환 교수 <그림설명> [그림 1] 스파이크(항원) 단백질, RNA 면역증강제, 그리고 아연 착화합물 기반의 RNA 안정화제로 이루어진 백신 플랫폼은 바이러스 표면의 스파이크 단백질에 대한 항체 생성 효율을 높여 면역을 형성한다.
- 27
- 작성자뇌의약연구단 금교창 박사팀
- 작성일2020.04.16
- 조회수9236
-
26
인공 시각 최적화에 한 발짝 더 다가섰다
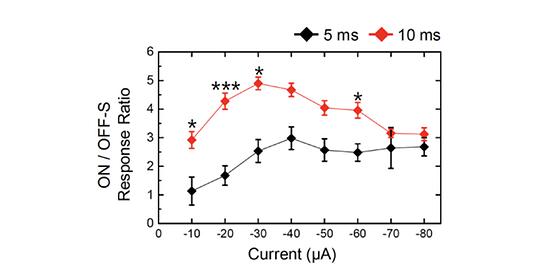
- 쥐 망막의 신경세포 실험 통해 인공 시각 구현을 위한 최적의 전기 자극 확인 - 인공 망막 장치에 적용하여, 보다 자연스러운 고품질 인공 시각 구현 기대 한국과학기술연구원(KIST, 원장 이병권) 바이오마이크로시스템연구단 임매순 박사팀은 실험용 쥐의 망막에서 신경 세포를 전기적으로 자극할 때 자연스러운 인공 시각을 만드는 최적의 전류 크기가 있음을 확인하고, 인공 망막 장치의 성능을 향상시킬 수 있는 방법을 개발했다고 밝혔다. 망막 변성 질환에는 상실된 시력을 되찾을 수 있는 치료 약물이 존재하지 않는다. 이식이 가능한 안구 앞면의 각막과 달리 안구 뒤편의 망막은 뇌 일부분인 복잡한 신경 조직이어서 이식이 불가능하다. 현재 시력을 되찾을 수 있는 유일한 방법은 망막 표면에 마이크로 전극을 이식하여 망막의 살아남은 신경 세포를 전기적으로 자극하는 인공 망막 장치이다. 망막은 복잡한 신경망을 이용해 영상 정보를 여러 종류의 망막 신경절 세포에 압축한 후 뇌로 전송한다. 이 과정에서 특정 시공간에서 밝기가 증가할 때는 ON 세포가 밝기가 감소할 때는 OFF 세포가 반응하여 뇌에 정보를 전달한다. 정상 망막에서는 ON 세포와 OFF 세포가 빛에 의해 각각 따로 활성화되지만 인공 망막에서 사용되는 전기 자극으로는 모든 신경절 세포가 동시에 활성화되는 것이 현재 인공 망막 기술의 큰 문제점이었다. 밝아졌을 때 반응해야 할 ON 세포와 어두워졌을 때 반응해야 할 OFF 세포가 전기 자극에 의해 동시에 정보를 전송하면 뇌는 그 의미가 헷갈릴 수밖에 없다. 따라서, 원하는 종류의 망막 신경절 세포를 얼마나 선택적으로 활성화할 수 있느냐가 인공 시각의 품질에 영향을 줄 수 있는 중요한 지표로 여겨지고 있다. 지금까지는 최적의 전기 자극 방법(자극 반복 주기, 전류 파형 모양, 전류 세기 등)을 결정하기 위해 인공 망막 장치를 이식받은 환자에게 직접 물어보는 방법이 주로 사용되었으나 실험동물을 이용한 기초실험은 많이 부족했다. KIST 연구진은 실험용 쥐의 망막에서 전류의 크기를 바꿔가며 ON 신경절 세포와 OFF 신경절 세포가 어떻게 반응하는지 근본적인 연구에 집중했다. 연구진은 ON 세포들의 신경 신호는 전류 크기에 따라 민감하게 변하지만, OFF 세포들에서는 덜 민감하게 변하는 것을 확인했다. OFF 세포 대비 ON 세포들의 신경 신호를 최대화하는 최적의 전류 값을 찾아내었고, ON 세포를 선택적으로 활성화시킬 수 있게 됐다. KIST 임매순 박사는 “최적의 전류 크기로 망막을 자극하면 뇌가 해석하기 쉬운 자연스러운 인공 시각을 형성하기에 적합하다는 것을 의미한다.”라며, “현재 사람의 망막 색소 변성에 해당하는 질병을 겪는 실험용 쥐를 대상으로 추가적인 실험을 진행하고 있다.”라고 말했다. 또한, “이번 연구 성과와 함께 신경과학에 기반한 새로운 구조의 마이크로 전극 개발을 통해 인공 망막 장치의 성능을 획기적으로 개선하기 위한 융·복합 원천 기술을 개발하고 있다.”라고 말했다. 본 연구는 과학기술정보통신부(장관 최기영) 지원으로 KIST의 기관 주요사업으로 수행되었으며, 연구 결과는 「미국전기전자공학회 신경 시스템 및 재활 공학 회보 (IEEE Transactions on Neural Systems and Rehabilitation Engineering)」 (IF : 3.85, JCR 분야 상위 3.97%) 최신호에 게재되었다. * (논문명) Optimal electric stimulus amplitude improves the selectivity between responses of ON versus OFF types of retinal ganglion cells - (제1저자) 하버드 의대, 매사추세츠 종합병원 이재익 박사후연구원 - (교신저자) 한국과학기술연구원 바이오마이크로시스템연구단 임매순 선임연구원 <그림설명> [그림 1] 전기 자극의 전류 크기에 따른 OFF 세포 대비 ON 세포의 신경 신호 크기 비교 결과. 두 자극 지속 시간(5밀리세컨드, 10밀리세컨드)에서 모두 중간 크기의 전류(-30 또는 ?40㎂)에서 반응 크기의 비율이 최고가 되며, 다른 전류와 비교하면 최적의 전류 값에서 선택비가 2배에서 3배 정도로 향상됨.
- 25
- 작성자바이오마이크로시스템연구단 임매순 박사팀
- 작성일2019.10.11
- 조회수9439
-
24
신경회로 조절하는 초소형 다기능 브레인 칩 개발
- 생쥐 뇌에 약물전달해 기억회로 조절, 뇌기능 정밀 조절 응용 기대 KIST 조일주 박사 연구팀은 뇌의 여러 부위에서 발생하는 신경신호를 동시에 측정하는 한편 약물이나 빛을 전달할 수 있는 초소형 브레인 칩을 개발했다고 22일 밝혔다. 뇌에 대한 이해를 통해 뇌질환을 정복하거나 뇌기능을 증강시키기 위해서는 뇌에서 발생하는 신호를 세포 하나하나 수준에서 정밀하게 측정해야 한다. 때문에 뇌에 칩을 삽입하거나 비침습적 영상기술로 신경신호를 측정하려는 연구가 활발하다. 이는 감지한 신경신호를 통해 생각을 읽어 동작이나 언어표현 없이도 기계를 움직이고자 하는 뇌-기계 인터페이스 시스템(brain?machine interfaces, BMIs)의 핵심기술이기도 해 더욱 주목받는다. 브레인 칩을 통해 뇌에서 나오는 신호를 읽어 뇌 기능의 이상을 확인하는 것은 가능했으나 반대로 뇌에 신호를 보내는 양방향 소통은 아직 많이 연구되지 않았다. 뇌기능을 제어하기 위해 파킨슨씨병 환자 등을 대상으로 심부자극술을 위한 칩이 사용되고 있으나 뇌 회로의 정밀한 자극이나 뇌신호 변화의 동시 측정은 어려웠다. 연구진은 머리카락 굵기의 아주 얇은(40마이크로미터 두께) 초소형 브레인칩을 개발하고 이를 살아있는 생쥐의 뇌에 삽입하여 생쥐의 기억을 담당하는 해마 부위에 빛과 약물을 전달함으로써 뇌회로를 강화하거나 약화시킬 수 있음을 확인했다. 빛이나 약물 자극으로 기억을 담당하는 신경회로를 제어할 수 있음을 보여준 것이다. 또한 이 과정에서 해마 여러 부위에서 동시다발적으로 발생하는 광범위한 신경신호를 단일 세포수준에서 정밀하게 측정해냈다. 특히 이식시 조직손상이나 감염 가능성과 직결되는 요소인 소형화측면에서 눈에 띄는 성과를 얻었다. 약물이동채널과 광자극을 위한 광도파로(optical waveguide), 전기자극을 위한 전극, 뇌신호 측정전극을 모두 머리카락 굵기의 실리콘 구조체에 집적한 것이다. 기존 탐침 대비 6~8배 가까이 축소된 작은 크기의 탐침 4개와 32개의 전극이 내장되어 신경세포 하나하나로부터 신호를 읽어 들이고 약물이나 빛을 수 초 내 직접 전달했다. 이번 연구결과는 마취된 생쥐에서 이뤄진 것으로 연구진은 향후 깨어있는 생쥐를 대상으로 행동연구를 함께 추진할 계획이다. 조일주 박사는 “뇌기능을 정밀하게 조절할 수 있는 초소형 시스템을 개발한 것”이라며 “향후 기존 뇌회로 연구방법의 한계를 극복하고 뇌 기능 정밀조절 방법을 제시할 수 있을 것으로 기대된다”고 의의를 설명했다. <그림설명> 브레인칩을 구성하고 있는 다기능 탐침 어레이_(좌) 브레인 칩을 구성하고 있는 탐침 어레이의 확대 모습, (우) 광자극, 약물자극, 전기자극 및 신호 측정 기능이 집적된 초소형 브레인칩이 패키징된 모습 다기능 브레인칩의 개념도_4개의 탐침에서 광자극, 약물전달 등의 자극과 신경신호 측정을 통하여 신경세포간의 연결을 확인하는 모습을 보여주는 개념도
- 23
- 작성자바이오마이크로시스템연구단 조일주 박사팀
- 작성일2019.08.26
- 조회수8347
-
22
반도체가 냄새를 맡는다? ‘세포’를 모사한 ’초민감·감각 센싱 플랫폼‘ 개발
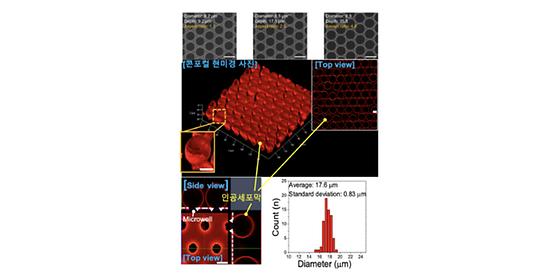
- 생체 기관의 구조와 유사한 3차원 인공 세포구조물 집적 칩 최초 제작 - 생체 감각기관 모사 초민감 인공 오감 센싱 플랫폼으로 응용 기대 한국과학기술연구원(KIST, 원장 이병권) 뇌과학연구소 바이오마이크로시스템 연구단 김태송 단장 연구팀은 국민대학교 화학과 유연규 교수팀과의 공동연구를 통해 반도체의 주된 재료인 실리콘 기판 위에 수만 개 이상의 3차원 인공세포막을 제작하는 기술을 개발했다고 밝혔다. 또한, 이 인공세포막 표면에 이온 채널* 단백질을 결합하여, 특정 조건을 감지하면 이온 채널이 열리고, 신호를 발생시키는 것을 확인했다. *이온 채널 : 생체막을 관통하는 구멍을 형성하여 생체막 내외의 이온을 통과시키는 단백질 분자. 예를 들어 후각세포의 경우 특정 이온이 채널을 통과하여 전기신호를 만듦으로써 뇌에서 냄새를 인식하게 함 포유동물은 개체마다 특유의 감각 기능을 보유하고 있다. 예를 들어, 개는 인간보다 약 1000배 이상 민감한 후각을 보유하고 있다. 이는 개의 후각세포와, 냄새를 구별하는 이온 채널의 숫자가 훨씬 많기 때문이다. 만약 이들 후각세포를 인공적으로 반도체 소자와 같은 초소형 칩 위에 구현할 수 있다면 공항에서 개를 훈련해 폭발물이나 마약과 같은 금지약물의 검사에 동원하지 않고도 아주 정밀하고 손쉽게 검사함으로써 재난과 위험으로부터 보호할 수 있을 것이다. 지금까지 인공세포막은 시계보다 정확히 이루어지는 생명체의 생명현상을 밝히거나, 생명현상에 관여하는 특정 반응을 밝히기 위한 모델실험, 새로운 약물을 개발하기 위한 사용 등으로 전 세계적으로 큰 관심의 대상이 되어왔다. 그러나 현재까지의 연구결과는 생체환경과 유사한 액체에 떠 있는 세포 모양의 인공 세포(GUV**)를 이용한 것으로, 고체 기판 위에 고정된 인공세포막을 이용한 것이 아니었다. 고체에 고정된 막으로서의 연구는 2차원의 평평한 막을 이용한 방법이 발표되고 있으나, 넓은 표면적을 갖기에는 막의 안정성이 떨어져 인공세포막의 생존시간이 24시간 정도에 불과하여 초민감·감각 센싱 플랫폼으로써 응용하기에 부족한 수준이다. **GUV(Giant Unilamellar Vesicle) : 이중막인 인공세포막으로 이루어진 구형(sphere) 형태의 구조물을 일컬으며 크기가 1~200㎛의 분포를 가짐 KIST 연구진은 이러한 기존의 한계점들을 극복하기 위해 실리콘 기판에 수만 개의 미세 구멍을 만들어 개개의 구멍 위에 균일하고 넓은 표면적을 갖는 3차원 인공세포(GUV) 구조물 제작 방법을 최초로 개발하였다. 특히, 5일 이상 구조물이 터지거나 변형되지 않고 유지될 수 있을 정도로 인공세포막의 안정성이 뛰어났다. 또한, 이 실리콘 기판 위에 제작된 3차원 인공세포막 구조물에 세로토닌*** 수용 채널을 다량 결합했다. 이 결합 된 채널들이 정상적으로 작동함을 확인하고, 이를 통해 제작한 인공세포막이 구조물로서 뿐만 아니라 세포의 기능도 정상적으로 수행할 수 있음을 밝혔다. 더 나아가 이를 응용하면 생명체만큼이나 민감하고 정확한 센서로 활용될 수 있음을 시사했다. ***세로토닌: 세로토닌은 뇌 신경계에 작용하는 신경전달물질의 하나로 행복을 느끼는 데에 기여한다고 일반적으로 알려져 있다. KIST 김태송 박사는 “이번 연구를 통해 개발된 기술은 아직도 우리가 알지 못하는 생명현상의 근원을 밝히기 위한 연구 플랫폼으로서뿐 아니라, 반도체 기판 위에 고정된 3D 인공 세포 집합체에 실제 개 코의 후각세포와 기능을 그대로 적용하여 마약이나 폭발물 같은 특정 물질을 인식하는 인공 개 코를 포함한 우수한 인공 오감 센싱 플랫폼으로 활용할 수 있다.”라고 말했다. 본 연구는 과학기술정보통신부(장관 유영민) 지원으로 KIST 주요사업으로 수행되었으며, 연구결과는 ‘Biosensors and Bioelectronics’ (IF : 9.518, JCR 분야 상위 0.595%)에 최신호에 게재되었다. * (논문명) Enhancement of membrane protein reconstitution on 3D free-standing lipid bilayer array in a microfluidic channel - (제 1저자) 한국과학기술연구원 한원배 박사(PostDoc.) - (교신저자) 한국과학기술연구원 김태송 책임연구원 [붙임] 연구결과 개요, 연구결과 문답, 용어 설명, 그림 설명, 연구진 이력 사항 <그림설명> <그림 1> (상) 실리콘 기판에 형성된 직경 8㎛ 홀 어레이 평면 및 단면, (중) 개개의 실리콘 홀 위에 형성된 구형상의 인공세포막 구조물 콘포컬 현미경 사진. 위쪽 및 옆쪽에서 본 인공세포막, (하 우측) 인공 세포구조물 크기 분포 그래프 <그림 2> 실리콘 기판 미세 홀(hole) 어레이 위에 형성된 구형의 3차원 인공 세포구조물 대면적 사진 (형광현미경 사진)
- 21
- 작성자바이오마이크로시스템연구단 김태송 박사팀
- 작성일2019.08.20
- 조회수8539
-
20
태아의 뇌신경 형성 과정에서 뇌세포의 성장 및 두뇌 크기 조절 메커니즘 밝혔다
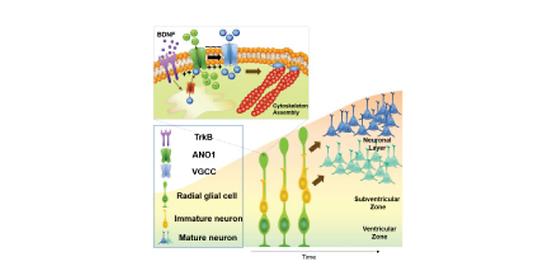
- KIST 오우택 소장 연구팀, 염소이온 채널 ‘아녹타민1’의 뇌 형성에서의 역할 규명 - 뇌세포의 분포 및 두뇌의 크기에 영향, 뇌 발달과 관련된 질병 이해 증진 한국과학기술연구원(KIST, 원장 이병권) 뇌과학연구소 오우택 소장, 홍규상 박사팀은 신경줄기세포*의 염소이온채널** ‘아녹타민1’이 태아의 신경 발달과정에서 대뇌의 뇌세포를 특정 위치로 이동시키고 두뇌의 크기를 조절한다고 밝혔다. *신경줄기세포(Neural Stem Cell): 자가 증식이 가능한 세포로 신경계통의 모든 세포로의 분화능력을 가짐 **염소이온채널(Chloride Ion Channel): 세포막에 존재하여 세포의 안·밖으로 염소 이온을 통과시키는 막단백질 선천적 뇌 신경세포의 발달 장애는 인지능력 저하, 운동기능 저하, 틱장애, 자폐증과 같은 다양한 뇌 관련 질병을 야기한다. 하지만 대뇌의 발달과정은 정밀하게 조절되고, 다양한 유전자와 환경 인자가 관여하기 때문에 그 원인을 알기가 어려운 실정이다. 최근 KIST 연구진은 태아의 신경 발달과정에서 신경줄기세포가 조절되는 메커니즘을 규명하여 신경발달장애의 근원을 이해하고, 두뇌가 어떻게 발달하는 지를 밝혔다. 신경줄기세포는 배아의 뇌에서 뉴런(신경세포)을 증식 시킬 뿐만 아니라 뇌 피질의 정확한 위치에 이동시켜 두뇌 형성 과정 전체를 조절하는 역할을 한다. 이 과정은 매우 정교하게 처리되는데, 신경줄기세포는 섬모라 불리는 긴 팔(긴 섬모)을 뇌의 끝부분까지 뻗고, 뉴런은 이 긴 팔을 마치 사다리처럼 타고 가서 제자리를 찾아가게 된다고 알려져 있다. 그러나 지금까지는 이러한 신경줄기세포가 뻗는 긴 섬모의 연장에 따른 뉴런의 이동 및 두뇌와의 연관성이 명확하게 규명되지 않았다. KIST 오우택·홍규상 박사팀은 전기 생리학, 면역학, 생화학적인 다양한 기법을 활용하여 ‘아녹타민1’ 유전자가 뇌신경세포의 발달과정 중 신경줄기세포에서 발현이 많이 되었음을 확인하였다. ‘아녹타민1’ 채널이 활성화되면 그 신호에 의해 신경줄기세포의 증식뿐만 아니라, 긴 섬모의 길이가 연장되고, 뇌신경 발달과정에서 대뇌 피질 내에 존재하는 뉴런들의 위치와 두뇌의 크기도 조절한다는 사실을 규명하였다. KIST 연구진은 ‘아녹타민1’이 결핍된 생쥐의 신경줄기세포의 섬모의 길이가 정상 생쥐보다 짧은 것을 확인하였고, 신경세포의 정상적 발달을 저해하여 최종 두뇌의 크기도 정상 생쥐에 비해 작아지는 것을 발견하였다. KIST 오우택 소장은 “뇌신경세포의 형성 과정 중 신경줄기세포에서 아녹타민1 이온채널의 역할을 재조명하였고, 동물의 뇌신경 형성 과정에서 생리학적인 이해의 범위를 한층 넓힐 수 있었다”며, “‘아녹타민1’ 이온채널 유전자의 역할을 명확하게 밝힌 연구를 통하여 두뇌 형성 과정에서의 오류로 인한 자폐증, 조현병 그리고 간질과 같은 뇌 질병을 이해하고, 그 치료를 위한 초석이 되는데 역할을 할 것이라 사료된다”고 연구의 의의를 밝혔다. 본 연구는 과학기술정보통신부(장관 유영민) 지원으로 한국연구재단 뇌과학원천기술개발사업, 리더연구자사업을 통해 수행되었으며, 연구결과는 미국 국립과학원 회보(PNAS, Proceedings of National Academy of Sciences, U.S.A.) (IF : 9.504, JCR 상위 : 7.031 % ) 최신호에 게재되었다. * (논문명) ANO1/TMEM16A regulates process maturation in radial glial cells in the developing brain - (제1저자) KIST 신경과학연구단 홍규상 선임연구원 중앙대학교 약학대학 이성훈 조교수 - (교신저자) KIST 뇌과학연구소 오우택 책임연구원 <그림설명> [그림 1] +/+: 일반마우스의 두뇌에서의 뉴런들 분포 -/- : 아녹타민1 녹아웃 마우스의 두뇌에서의 뉴런들 분포 일반마우스는 CUX1/NOR1로 표시된 레이어 마커안에 잘 분포되어 있으나, 아녹타민1이 결핍된 마우스는 경계없이 퍼져있는 것으로 확인되어, 제대로 뉴런들이 있어야할 곳에 위치되지 않았음 [그림 2] +/+: 일반마우스의 두뇌 크기(평균치) +/- 부모 중 한쪽의 염색체에만 아녹타민1 이 결핍된 경우 -/- : 부모 양쪽 모두 아녹타민1 결핍된 경우 +/-, -/- 모두 스탠다드 에러(일반적으로 정상으로 인정되는 오류의 범위)를 벗어난 두뇌 크기를 보여줌 [그림 3] 대표적 신경줄기세포인 Radil gila cell의 두뇌에서의 발달과정. BDNF 성장인자(BDNF가 TrkB리셉터에 결합하면 세포 내부에 칼슘이 생성되고 아녹타민1 이 활성화됨) 에 의한 아녹타민1의 활성화와 이에 따른 신경줄기세포 섬모의 조절 모식도.
- 19
- 작성자신경과학연구단 홍규상 박사팀
- 작성일2019.07.02
- 조회수9254
-
18
치매치료제, 기존 약물의 한계를 극복할 열쇠를 찾다
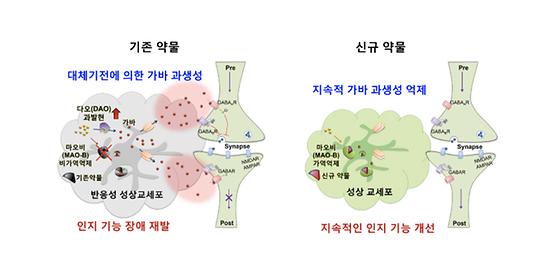
- 치매DTC융합연구단, 한계 극복한 새로운 패러다임의 치매 치료약물 개발 - 기존 약물의 실패 원인을 밝히고 이를 해결할 신규 치료 기전 규명 한국과학기술연구원(KIST, 원장 이병권) 치매DTC융합연구단 박기덕 박사 연구팀은 반응성교세포연구단 이창준 박사 연구팀(현, IBS)과의 융합연구를 통해 알츠하이머성 치매를 극복할 수 있는 새로운 패러다임의 연구결과를 발표하였다. KIST 연구진은 기존 약물의 한계를 극복 할 수 있는 신규 치매 치료 약물을 개발하였다. 이 신약은 알츠하이머 치매환자의 뇌에서 과생성되는 가바(GABA)*의 양을 줄일 수 있는 물질로, 가바로 인한 치매환자의 기억력 저하 및 인지 장애를 획기적으로 개선할 수 있는 치료 후보약물이다. *GABA : 포유류의 중추신경계에 생기는 억제성 신호 전달 물질로써, 반응성 성상교세포에서 가바가 과생성되면 기억력 저하나 인지 장애를 유발한다. KIST 연구진은 기존 약물들은 초기에는 가바의 양을 줄여주어 인지기능을 개선시킬 수 있었지만, 장기간 투여 시 생체 내 대체기전**이 작동하기 시작하면서 가바의 양이 다시 증가하고 인지 장애가 다시 생긴다는 사실을 규명했다. **대체기전 : 생체 내 주요 역할을 담당하는 기전이 억제되어 기능을 상실하였을 때 이를 대신해서 같은 역할을 할 수 있도록 작동되는 생체 내 보상기전 반면에, KIST 연구진이 개발한 후보약물은 장기간 투여 시에도 이러한 대체기전을 작동시키지 않음으로써 장기간 동안 지속적으로 인지기능을 개선시킬 수 있음을 확인하였다. 또한 알츠하이머병에 걸린 유전자 변이 실험용 쥐에 투여하여 다양한 행동실험을 통해 인지기능이 회복된 것을 확인했을 뿐 아니라, 적은 용량으로 장기간 투여한 시험에서도 월등한 인지기능 개선 효능을 확인하였다. 특히, 약물로서의 적합성(ADME/Tox)을 검증한 결과 이 신약 후보약물은 인체의 뇌 속으로 매우 높은 효율로 전달되었으며, 다른 신경계에 부작용이 없는 뛰어난 약물성을 나타냈다. 이번 연구결과는 과거 임상에서 단기적 효능을 보였음에도 결국 승인되지 못한 기존 약물의 실패 원인을 규명하였을 뿐만 아니라, 이러한 한계를 극복할 수 있어 주목받고 있다. KIST 박기덕 박사는 “개발된 후보약물은 치매에 의한 인지장애를 장기간 동안 지속적으로 개선시킬 수 있음이 확인되었다”며, “후보약물의 우수한 효능 뿐만아니라 뇌 투과율 및 인체 안전성이 뛰어나 장기간 진행되는 치매 치료약물 임상 시험에서 좋은 결과를 얻을 수 있을 것”이라고 밝혔다. 이는 국가과학기술연구회(NST, 이사장 원광연)에서 시행한 융합연구사업 가운데 KIST 치매DTC융합연구단 사업(단장 배애님)으로 수행되었다. 이번 연구결과는 세계적 학술지 사이언스의 자매지인 ‘Science Advances’ (IF: 11.51, JCR 분야 상위 5.47%) 최신호에 온라인 게재되었다. 본 후보약물은 2017년 ㈜메가바이오숲에 기술이전(선급금 5.5억원, 정액기술료 60억원, 경상기술료 3%) 되었으며, 현재 글로벌 신약개발을 위한 영장류 기반 전임상 시험이 진행 중이고, 2019년 하반기에 임상 시험 승인을 신청할 계획이다. *(논문명) Newly developed reversible MAO-B inhibitor circumvents the shortcomings of irreversible inhibitors in Alzheimer’s disease - (제1저자)한국과학기술연구원 박종현 연구원 - (교신저자)한국과학기술연구원 이창준 책임연구원(現 IBS 인지 및 사회성 연구단 공동단장) - (교신저자)한국과학기술연구원 박기덕 책임연구원 <그림설명> <그림1> 기존 약물의 단기 효능 한계와 이를 극복한 신규 치료약물의 지속적 효능 <그림2> 대체기전에 의한 기존 약물의 한계 및 이를 극복한 신규약물의 치료기전
- 17
- 작성자치매DTC융합연구단 박기덕 박사팀
- 작성일2019.03.25
- 조회수11309